
依诺生物结合mRNA的技术特征和药物设计发展趋势,将AI技术融合进mRNA药物设计,涵盖从靶点发现、蛋白质序列设计到mRNA序列设计的全流程。通过mRNA高通量合成设计序列进行验证提供的全面实时真实数据反馈和诸多产品开发案例真实数据积累,推动AI算法的持续迭代。依诺生物发展的AI和mRNA技术共同驱动的靶点发现和药物设计技术,不仅可以帮助客户针对已知蛋白质靶点的mRNA药物开发实现基于成药性的蛋白质与mRNA序列高效设计和自主知识产权突破,还可以进一步开展源头的靶点发现和筛选,推动各类创新mRNA药物的研究和开发。
靶点发现与蛋白质序列设计是mRNA药物开发的“核心基础和关键起点”,mRNA编码的目标蛋白质的功能直接决定mRNA药物治疗效果。特别是在癌症等复杂疾病中(如针对肿瘤新抗原),识别最优靶点并设计出具有高效生物活性和良好稳定性的蛋白质,是一项复杂且耗时的经验性工作。传统方法难以应对庞大的生物数据和复杂的蛋白质折叠机制,而AI则具备强大能力,可高效分析多维生物数据、精准预测蛋白结构并优化序列,从而显著降低研发风险、加快进程,助力新靶点发现和更优疗法设计。而对于真实数据验证反馈,传统的蛋白质技术平台因为蛋白质表达和纯化的技术限制导致近三分之二序列无法获得,从而无法实现全面有效的验证。mRNA技术可完美克服该限制,实现任一设计序列的合成与验证,提供全面的真实数据反馈,提高靶点发现效率和机率。
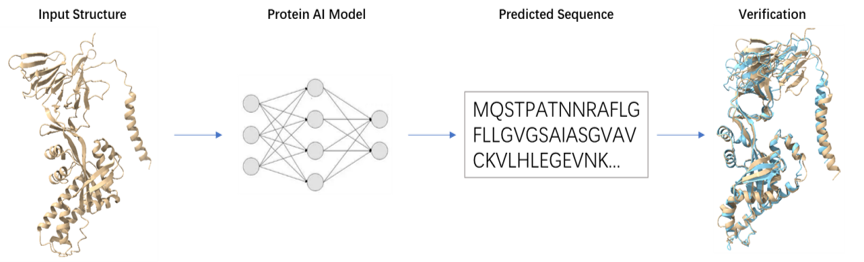
依诺生物开发的AI工具将功能模块(如抗原表位、酶切位点、信号肽、去免疫化设计模块)标准化,支持快速适应不同靶点与疾病场景的更进一步成药性优化需求,有效平衡了蛋白质的临床安全性与产业化需求,助力药物从研发到应用的高效转化。
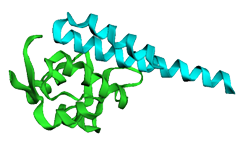
拥有本地部署的UniRef90、MGnify、PDB等蛋白结构及序列数据库
提供基于结构或序列的搜索比对服务
进化树构建服务


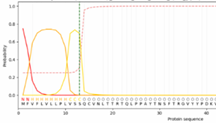
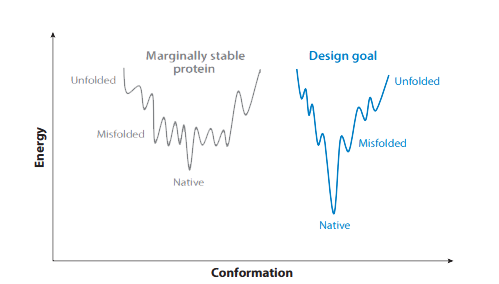
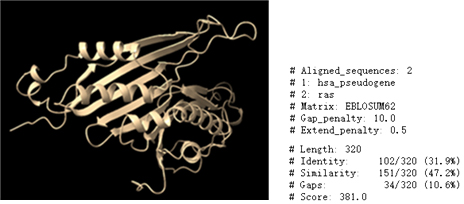
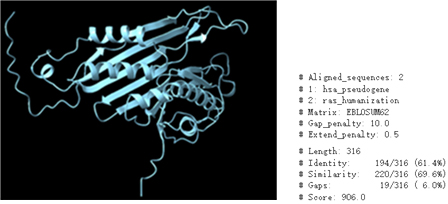
mRNA序列本身对药物的整体成药性也有至关重要的影响。精心设计的mRNA序列能够确保高效的翻译起始、良好的稳定性及可控的免疫原性,这些因素直接关系到蛋白质产量、表达持续时间以及治疗的安全性。由于密码子偏好性、mRNA二级结构以及编码区(CDS)与非翻译区(UTR)之间的复杂相互作用,mRNA序列的优化成为一项复杂任务。未优化的序列设计可能导致蛋白质表达量低、快速降解或不必要的免疫激活,从而影响治疗效果。人工智能技术为这种多层次的复杂性提供了有效的解决方案,实现了mRNA序列的精确多目标优化,最大化治疗效果并优化成药性。
依诺生物自主研发的AI序列优化算法 RheDesign,专注于编码区(CDS)的多维优化与功能转化,兼顾翻译效率、蛋白折叠能力与免疫兼容性,涵盖动态密码子使用建模、二级结构规避与重塑、功能导向的模块化设计等。实际应用中,RheDesign显著提升目标蛋白(如EGFP)表达量,表现出优于商业化工具的翻译效率与稳定性。该技术有效解决mRNA药物开发中翻译效率低和蛋白错误折叠等问题,为高表达、高活性的mRNA疫苗与治疗产品提供强有力支持。
AI序列优化算法 RheDesign 在实现CDS多维优化的基础上,进一步引入 UTR 联动设计,有效解决了传统独立设计CDS与UTR所带来的翻译不稳定、组织特异性差等问题,显著提升mRNA表达水平与功能一致性。针对某种细胞因子的表达,通过RheDesign设计mRNA序列相较传统方法可实现超过3倍的蛋白表达增强,尤其适用于高精度调控表达时序与靶向递送的mRNA疫苗和治疗药物开发,展现出更强的临床转化潜力与产业化优势。